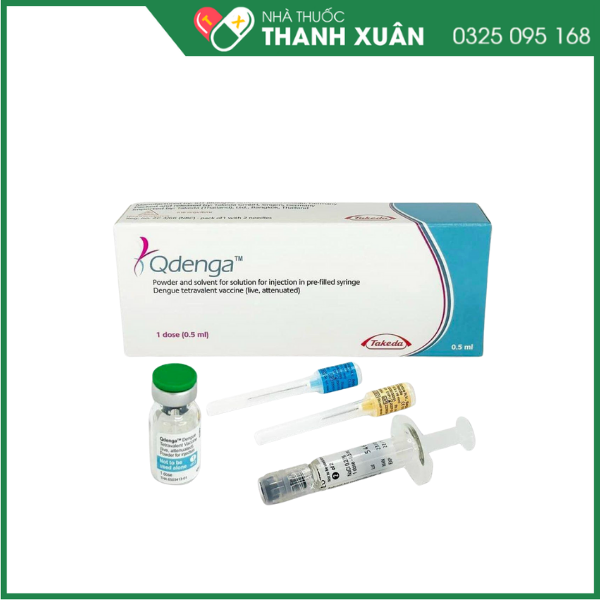
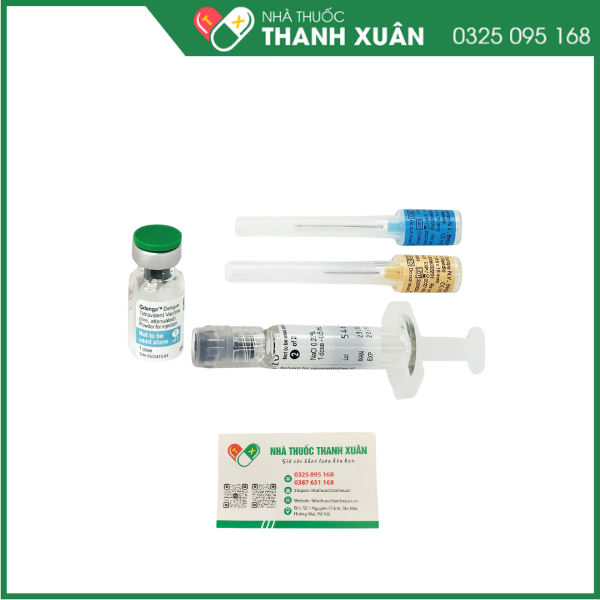
1. Thuốc Qdenga là thuốc gì?
Vắc xin Qdenga là chế phẩm sinh học đặc biệt có khả năng phòng bệnh sốt xuất huyết do virus Dengue gây ra, có khả năng bảo vệ chống lại cả 4 nhóm huyết thanh của virus dengue, bao gồm DEN-1, DEN-2, DEN-3 và DEN-4, được chỉ định tiêm cho người từ 4 tuổi trở lên với hiệu lực bảo vệ hơn 80% nguy cơ mắc bệnh do 4 tuýp virus Dengue và trên 90% nguy cơ nhập viện, mắc bệnh nặng và biến chứng nguy hiểm do bệnh sốt xuất huyết gây ra.
2. Thành phần thuốc Qdenga
Sau khi hoàn nguyên, 1 liều (0,5 ml) chứa:
Tuýp huyết thanh 1 virus Dengue (virus sốt xuất huyết) (sống, giảm độc lực)*: ≥3,3 log10
PFU**/liều
Tuýp huyết thanh 2 virus Dengue (sống, giảm độc lực)#: ≥ 2,7 log10 PFU**/liều
Tuýp huyết thanh 3 virus Dengue (sống, giảm độc lực)*: ≥ 4,0 log10 PFU**/liều
Tuýp huyết thanh 4 virus Dengue (sống, giảm độc lực)*: > 4,5 log10 PFU**/liều
*Được sản xuất trong tế bào Vero bằng công nghệ DNA tái tổ hợp. Các gen của protein bề mặt đặc hiệu tuýp huyết thanh được thiết kế thành bộ khung của virus Dengue tuýp 2. Sản phẩm này chứa các sinh vật biến đổi gen (GMO).
#Được sản xuất trong tế bào Vero bằng công nghệ DNA tái tổ hợp
**PFU = Đơn vị hình thành mảng bám (Plaque-forming units)
3. Dạng bào chế
Bột và dung môi pha dung dịch tiêm.
Trước khi hoàn nguyên, vắc-xin ở dạng bột hoặc bánh đông khô màu trắng đến trắng ngà.
Dung môi là dung dịch trong suốt, không màu.
4. Chỉ định
Qdenga® được chỉ định để phòng ngừa bệnh sốt xuất huyết ở những người từ 4 tuổi trở lên.
Việc sử dụng Qdenga® phải phù hợp với khuyến cáo chính thức.
5. Liều dùng
Liều lượng
Người từ 4 tuổi trở lên
Qdenga® nên được dùng dưới dạng liều 0,5 ml theo lịch trình hai liều (0 và 3 tháng).
Nhu cầu về liều tăng cường chưa được thiết lập.
Nhóm bệnh nhân trẻ em khác (trẻ em <4 tuổi)
Độ an toàn và hiệu lực của Qdenga® ở trẻ em dưới 4 tuổi chưa được xác định.
Dữ liệu hiện có được mô tả nhưng không đưa ra khuyến cáo nào về chất lượng.
Người cao tuổi
Không cần điều chỉnh liều ở người cao tuổi ≥ 60 tuổi.
Cách dùng
Sau khi hoàn thành việc hoàn nguyên vắc-xin đông khô với dung môi, Qdenga® phải được tiêm dưới da, tốt nhất là ở phần trên cánh tay trong vùng cơ delta.
Không tiêm tĩnh mạch, tiêm trong da hay tiêm bắp Qdenga®.
Không được trộn vắc-xin này trong cùng một ống tiêm với bất kỳ vắc-xin hoặc thuốc tiêm nào
khác.
Hướng dẫn hoàn nguyên vắc-xin với dung môi có trong lọ
Qdenga® là loại vắc-xin gồm 2 thành phần, bao gồm 1 lọ chứa vắc-xin đông khô và 1 lọ chứa dung môi. Vắc-xin đông khô phải được hoàn nguyên bằng dung môi trước khi dùng.
Chỉ sử dụng ống tiêm vô khuẩn để hoàn nguyên và tiêm Qdenga®. Không được trộn Qdenga® với các vắc-xin khác trong cùng một ống tiêm.
Để hoàn nguyên Qdenga®, chỉ sử dụng dung môi (dung dịch natri chloride 0,22%) được cung cấp cùng với vắc-xin vì nó không có chất bảo quản hoặc các chất kháng virus khác. Cần tránh tiếp xúc với chất bảo quản, chất sát khuẩn, chất tẩy rửa và các chất kháng virus khác vì chúng có thể làm bất hoạt vắc-xin.
Lấy lọ vắc-xin và lọ dung môi ra khỏi tủ lạnh và đặt ở nhiệt độ phòng trong khoảng 15 phút.
• Tháo nắp cả hai lọ và làm sạch bề mặt của nút chặn trên đầu lọ bằng cách sử dụng miếng gạc tẩm cồn.
• Gắn kim vô khuẩn vào ống tiêm vô khuẩn 1 ml và đâm kim vào lọ dung môi. Kim được khuyên dùng là 23G.
• Từ từ ấn pittông xuống hoàn toàn.
• Lật ngược lọ, rút toàn bộ lượng chứa bên trong lọ và tiếp tục kéo pittông ra đến 0,75 ml. Một bọt khí nên được nhìn thấy bên trong ống tiêm.
• Xoay ngược ống tiêm để đưa bọt khí trở lại pittông.
• Đâm kim của cụm ống tiêm vào lọ vắc-xin đông khô.
• Hướng dòng chảy của dung môi về phía thành lọ trong khi từ từ kéo lùi pittông để giảm khả năng hình thành bọt khí.
• Thả ngón tay của bạn ra khỏi pittông và giữ cụm ông tiêm trên một bề mặt phẳng, nhẹ nhàng xoay lọ theo cả hai hướng với cụm ống tiêm có kim được gắn vào.
• KHÔNG LẮC. Bọt và bọt khí có thể hình thành trong sản phẩm đã hoàn nguyên
• Để yên lọ và cụm ống tiêm một lúc cho đến khi dung dịch trở nên trong suốt. Quá trình này mất khoảng 30-60 giây.
Sau khi pha, dung dịch thu được phải trong suối, không màu đến vàng nhạt và về cơ bản không có các tiểu phân lạ. Loại bỏ vắc-xin nếu có tiểu phân và/hoặc nếu vắc-xin bị đổi màu.
• Rút toàn bộ thể tích dung dịch Qdenga® đã pha bằng cùng một ống tiêm cho đến khi một bọt khí xuất hiện trong ống tiêm.
• Lấy cụm ống tiêm có kim ra khỏi lọ.
• Giữ ống tiêm với kim hướng lên trên, gõ nhẹ vào thành của ống tiêm để đưa bọt khí lên trên cùng,
Vắc-xin đã hoàn nguyên
loại bỏ kim đi kèm và thay thế bằng kim vô khuẩn mới, đuổi bọt khí cho đến khi một giọt nhỏ chất lỏng hình thành ở đầu kim. Kim được khuyên dùng là 25G 16 mm.
• Qdenga® đã sẵn sàng để dùng bằng cách tiêm dưới da.
Qdenga® nên được sử dụng ngay sau khi hoàn nguyên. Độ ổn định về lý hóa trong khi sử dụng đã được chứng minh trong 2 giờ ở nhiệt độ phòng (lên đến 32,5°C) kể từ thời điểm hoàn nguyên lọ vắc-xin. Sau khoảng thời gian này, vắc-xin phải được loại bỏ. Không được trả Qdenga® trở lại vào tủ lạnh. Theo quan điểm vi sinh học, Qdenga® cần được sử dụng ngay. Nếu không dùng ngay, thời gian bảo quản và điều kiện bảo quản trong khi sử dụng là trách nhiệm của người sử dụng.
Hướng dẫn hoàn nguyên vắc-xin với dung môi có trong ống tiêm đóng sẵn dung môi
Qdenga® là loại vắc-xin gồm 2 thành phần, bao gồm 1 lọ chứa vắc-xin đông khô và dung môi được cung cấp trong ống tiêm đóng sẵn dung môi. Vắc-xin đông khô phải được hoàn nguyên bằng dung môi trước khi dùng.
Không được trộn Qdenga® với các vắc-xin khác trong cùng một ống tiêm.
Để hoàn nguyên Qdenga, chỉ sử dụng dung môi (dung dịch natri chloride 0,22%) trong ống tiêm đóng sẵn dung môi được cung cấp cùng với vắc-xin vì nó không có chất bảo quản hoặc các chất kháng virus khác. Cần tránh tiếp xúc với chất bảo quản, chất sát khuẩn, chất tẩy rửa và các chất kháng virus khác vì chúng có thể làm bất hoạt vắc-xin.
Lấy lọ vắc-xin và ống tiêm đóng sẵn dung môi ra khỏi tủ lạnh và đặt ở nhiệt độ phòng trong khoảng 15 phút.
• Tháo nắp khỏi lọ vắc-xin và làm sạch bê mặt của nút chặn trên đầu lọ bằng cách sử dụng miếng gạc tẩm cồn.
• Gắn kim vô khuẩn vào ống tiêm đóng sẵn dung môi và đâm kim vào lọ vắc-xin. Kim được khuyên dùng là 23G.
Lọ vắc-xin đông khô
• Hướng dòng chảy của dung môi về phía thành lọ trong khi từ từ kéo lùi pittông để giảm khả năng hình thành bọt khí.
• Thả ngón tay của bạn ra khỏi pittông và giữ cụm ống tiêm trên một bề mặt phẳng, nhẹ nhàng xoay lọ theo cả hai hướng với cụm ống tiêm có kim được gắn vào.
• KHÔNG LẮC. Bọt và bọt khí có thể hình thành trong sản phẩm đã pha.
• Để yên lọ và cụm ống tiêm một lúc cho đến khi dung dịch trở nên trong suốt. Quá trình này mất khoảng 30-60 giây.
Sau khi hoàn nguyên, dung dịch thu được phải trong suốt, không màu đến vàng nhạt và về cơ bản không có các tiểu phân lạ. Loại bỏ vắc-xin nếu có tiểu phân và/hoặc nếu vắc-xin bị đổi màu.
• Rút toàn bộ thể tích dung dịch Qdenga® đã hoàn nguyên bằng cùng một ống tiêm cho đến khi một bọt khí xuất hiện trong ống tiêm.
• Lấy cụm ống tiêm có kim ra khỏi lọ. Giữ ống tiêm với kim hướng lên trên, gõ nhẹ vào thành của ống tiêm để đưa bọt khí lên trên cùng, loại bỏ kim đi kèm và thay thế bằng kim vô khuẩn mới, đuổi bọt khí cho đến khi một giọt nhỏ chất lỏng hình thành ở đầu kim. Kim được khuyên dùng là 25G 16 mm.
• Qdenga® đã sẵn sàng để dùng bằng cách tiêm dưới da.
Qdenga® nên được sử dụng ngay sau khi hoàn nguyên. Độ ổn định về lý hóa trong khi sử dụng đã được chứng minh trong 2 giờ ở nhiệt độ phòng (lên đến 32,5°C) kể từ thời điểm hoàn nguyên lọ vắc-xin. Sau khoảng thời gian này, vắc-xin phải được loại bỏ. Không được trả Qdenga® trở lại vào tủ lạnh. Theo quan điểm vi sinh học, Qdenga® cần được sử dụng ngay. Nếu không dùng ngay, thời gian bảo quản và điều kiện bảo quản trong khi sử dụng là trách nhiệm của người sử dụng.
Bất kỳ phần thuốc nào không dùng hoặc vật liệu thải đi phải được loại bỏ theo đúng quy định của địa phương.
6. Chống chỉ định
• Quá mẫn với hoạt chất hoặc với bất kỳ tá dược nào hoặc quá mẫn với liều Qdenga® trước đó.
• Những người bị suy giảm miễn dịch bẩm sinh hoặc mắc phải, bao gồm cả điều trị ức chế miễn dịch như hóa trị liệu hoặc corticosteroid đường toàn thân liều cao (ví dụ prednisone 20 mg/ngày hoặc 2 mg/kg thể trọng/ngày trong 2 tuần hoặc hơn) trong vòng 4 tuần trước khi tiêm chủng, cũng như với các vắc-xin sống giảm độc lực khác.
• Những người bị nhiễm HIV có triệu chứng hoặc nhiễm HIV không có triệu chứng khi có kèm theo bằng chứng về suy giảm chức năng miễn dịch.
• Phụ nữ có thai.
• Phụ nữ cho con bú.
7. Tác dụng phụ
Tóm tắt hồ sơ về an toàn
Trong các nghiên cứu lâm sàng, các phản ứng được báo cáo thường xuyên nhất ở các đối tượng từ 4-60 tuổi là đau tại chỗ tiêm (50%), nhức đầu (35%), đau cơ (31%), ban đỏ tại chỗ tiêm (27%), khó chịu (24%), suy nhược (20%) và sốt (11%).
Những phản ứng bất lợi này thường xảy ra trong vòng 2 ngày sau khi tiêm, có mức độ từ nhẹ đến trung bình, trong thời gian ngắn (1-3 ngày) và ít gặp hơn sau lần tiêm Qdenga® thứ hai so với lần tiêm đầu tiên.
Xuất hiện virus có trong vắc-xin trong máu
Trong nghiên cứu lâm sàng DEN-205, virus trong vắc-xin xuất hiện trong máu thoáng qua đã được quan sát thấy sau khi tiêm chủng bằng Qdenga ở 49% người tham gia nghiên cứu chưa từng bị nhiễm sốt xuất huyết trước đó và ở 16% người tham gia nghiên cứu đã từng bị nhiễm
sốt xuất huyết trước đó. Sự có mặt virus có trong vắc-xin trong máu thường bắt đầu vào tuần thứ hai sau lần tiêm đầu tiên và có thời gian trung bình là 4 ngày. Virus trong vắc-xin có trong máu có liên quan đến các triệu chứng thoáng qua, nhẹ đến trung bình như nhức đầu, đau khớp, đau cơ và phát ban ở một số đối tượng. Sự có mặt của virus trong vắc-xin trong máu hiếm khi được phát hiện sau liều thứ 2.
Bảng liệt kê các phản ứng bất lợi
Các phản ứng bất lợi liên quan đến Qdenga® thu được từ các nghiên cứu lâm sàng được lập thành bảng dưới đây (Bảng 1).
Hồ sơ về an toàn được trình bày dưới đây dựa trên một phân tích gộp bao gồm 14.627 người tham gia nghiên cứu từ 4-60 tuổi (13.839 trẻ em và 788 người lớn) đã được tiêm chủng bằng
Qdenga®. Phân tích này bao gồm một phân nhóm nghiên cứu về tính gây phản ứng ở 3.830 người tham gia (3.042 trẻ em và 788 người lớn).
Phản ứng bất lợi được liệt kê theo các loại tần suất sau:
Rất thường gặp: ≥ 1/10
Thường gặp: ≥ 1/100 đến < 1/10
Ít gặp: ≥ 1/1.000 đến < 1/100
Hiếm gặp: ≥ 1/10.000 đến < 1/1.000
Rất hiếm gặp: < 1/10.000
Bảng 1: Phản ứng bất lợi từ các nghiên cứu lâm sàng (từ 4-60 tuổi)
|
Nhóm hệ cơ quan theo MedDRA |
Tần suất |
Phản ứng bất lợi |
|
Nhiễm khuẩn và nhiễm ký sinh trùng |
Rất thường gặp |
Nhiễm khuẩn đường hô hấp trên* |
|
Thường gặp |
Viêm mũi họng |
|
|
Ít gặp |
Viêm họng-viêm amidan** |
|
|
Rối loạn chuyển hóa dinh dưỡng |
Rất thường gặp |
Giảm sự ngon miệng*** |
|
Rối loạn tâm thần |
Rất thường gặp |
Dễ bị kích thích*** |
|
Rối loạn hệ thần kinh |
Rất thường gặp |
Nhức đầu, Buồn ngủ *** |
|
Ít gặp |
Chóng mặt |
|
|
Rối loạn hệ tiêu hoá |
Ít gặp |
Tiêu chảy, Buồn nôn, Đau bụng, Nôn |
|
Rối loạn da và mô dưới da |
Ít gặp |
Phát ban****, Ngứa*****, Nổi mề đay |
|
Rất hiếm gặp |
Phù mạch |
|
|
Rối loạn hệ cơ xương và mô liên kết |
Rất thường gặp |
Đau cơ |
|
Thường gặp |
Đau khớp |
|
|
Rối loạn toàn thân và tình trạng tại chỗ tiêm |
Rất thường gặp |
Đau, Ban đỏ tại chỗ tiêm, Khó chịu, Suy nhược, Sốt |
|
Thường gặp |
Sưng tại chỗ tiêm, Bầm tím tại chỗ tiêm*****, Ngứa tại chỗ tiêm*****, Bệnh giống cúm |
|
|
Ít gặp |
Xuất huyết, Đổi màu tại chỗ tiêm*****, Mệt mỏi***** |
* Bao gồm nhiễm khuẩn đường hô hấp trên và nhiễm khuẩn đường hô hấp trên do virus.
** Bao gồm viêm họng-amidan và viêm amidan
*** Thu thập ở trẻ em dưới 16 tuổi và các nghiên cứu lâm sàng.
**** Bao gồm ban, ban do virus, ban dát sần, ban ngứa.
***** Được báo cáo ở người lớn trong các nghiên cứu lâm sàng.
Nhóm bệnh nhân trẻ em
Dữ liệu trên trẻ em ở các đối tượng từ 4-17 tuổi:
Hiện có dữ liệu an toàn gộp từ các thử nghiệm lâm sàng đối với 13.839 trẻ em (9.210 trẻ từ 4-
11 tuổi và 4.629 trẻ từ 12-17 tuổi). Điều này bao gồm dữ liệu về tính gây phản ứng được thu thập ở 3.042 trẻ em (1.865 trẻ từ 4-11 tuổi và 1.177 trẻ từ 12-17 tuổi).
Tần suất, loại và mức độ nặng của các phản ứng bất lợi ở trẻ em phần lớn phù hợp với ở người lớn. Các phản ứng bất lợi được báo cáo thường gặp hơn ở trẻ em so với người lớn là sốt (11% so voi 3%), nhiễm khuẩn đường hô hấp trên (11% so với 3%), viêm mũi họng (6% so với 0,6%), viêm họng-amidan (2% so với 0,3%) và bệnh giống cúm (1% so với 0,1%). Các phản ứng bất lợi được báo cáo ít gặp hơn ở trẻ em so với người lớn là ban đỏ tại chỗ tiêm (2% so với 27%), buồn nôn (0,03% so với 0,8%) và đau khớp (0,03% so với 1%).
Các phản ứng sau đây đã được thu thập ở 357 trẻ em dưới 6 tuổi được tiêm chủng Qdenga®:
giảm sự ngon miệng (17%), buồn ngủ (13%) và dễ bị kích thích (12%).
Dữ liệu trên trẻ em ở các đối tượng dưới 4 tuổi, tức là ngoài chỉ định về độ tuổi:
Tính gây phản ứng ở các đối tượng dưới 4 tuổi đã được đánh giá ở 78 đối tượng được tiêm ít nhất một liều Qdenga®, trong đó 13 đối tượng được dùng phác đồ 2 liều theo chỉ định. Các phản ứng được báo cáo với tần suất rất thường gặp là dễ bị kích thích (25%), sốt (17%), đau tại chỗ tiêm (17%) và mất sự ngon miệng (15%). Buồn ngủ (8%) và ban đỏ tại chỗ tiêm (3%) được báo cáo với tần suất thường gặp. Sưng tại chỗ tiêm không được quan sát thấy ở những đối tượng dưới 4 tuổi.
Báo cáo các phản ứng bất lợi nghi ngờ
Báo cáo các phản ứng bất lợi nghi ngờ sau khi có giấy phép lưu hành thuốc là điều quan trọng.
Điều này cho phép theo dõi liên tục cân bằng lợi ích/nguy cơ của thuốc.
Thông báo cho bác sĩ các tác dụng không mong muốn bạn gặp phải khi sử dụng thuốc.
8. Tương tác thuốc.
Đối với những bệnh nhân đang được điều trị bằng globulin miễn dịch hoặc các sản phẩm máu có chứa globulin miễn dịch, như máu hoặc huyết tương, khuyến cáo nên chờ ít nhất 6 tuần và tốt nhất là 3 tháng sau khi kết thúc điều trị trước khi dùng Qdenga® để tránh trung hòa các virus giảm độc lực có trong vắc-xin.
Không nên tiêm Qdenga® cho những người đang được điều trị ức chế miễn dịch như hóa trị liệu hoặc corticosteroid đường toàn thân liều cao trong vòng 4 tuần trước khi tiêm chủng.
Sử dụng với các vắc-xin khác
Nếu Qdenga® được dùng đồng thời với một vắc-xin dạng tiêm khác, các vắc-xin phải luôn được tiêm tại các vị trí tiêm khác nhau.
Qdenga® có thể được dùng đồng thời với vắc-xin viêm gan A. Việc dùng đồng thời đã được nghiên cứu ở người lớn.
Qdenga® có thế được dùng đồng thời với vắc-xin sốt vàng. Trong một nghiên cứu lâm sàng bao gồm khoảng 300 đối tượng người lớn đã dùng Qdenga® đồng thời với vắc-xin sốt vàng. Đáp ứng kháng thể kháng virus Dengue đã giảm sau khi tiêm đồng thời vacxin Qdenga® và vacxin sốt vàng 17D. Chưa rõ ý nghĩa lâm sàng của phát hiện này.
9. Thận trọng khi sử dụng
Khuyến cáo chung
Phản vệ
Cũng như với tất cả các vắc-xin dạng tiêm khác, cần phải luôn có sẵn các phương tiện điều trị và giám sát y khoa thích hợp trong trường hợp có phản ứng phản vệ hiếm gặp sau khi tiêm vắc-xin.
Xem xét tiền sử y khoa
Cần phải xem xét tiền sử y khoa của từng cá nhân trước khi tiêm chủng (đặc biệt là liên quan đến tiêm chủng trước đó và các phản ứng quá mẫn có thể có đã xảy ra sau khi tiêm chủng).
Bệnh đồng thời
Nên hoãn tiêm Qdenga® ở những người đang sốt cao cấp tính. Không nên trì hoãn tiêm chủng nếu bị nhiễm khuẩn nhẹ, như cảm lạnh.
Đáp ứng miễn dịch bảo vệ có thế không được thể hiện ở tất cả các đối tượng được tiêm vắc-xin Qdenga® chống lại tất cả các tuýp huyết thanh virus Dengue và có thể giảm dần theo thời gian (xem phần 4.1). Hiện chưa rõ liệu việc thiếu sự bảo vệ có thể dẫn đến tăng mức độ nặng của bệnh sốt xuất huyết hay không. Khuyến cáo nên tiếp tục các biện pháp bảo vệ cá nhân chống lại muỗi đốt sau khi tiêm chủng. Các cá nhân nên tìm kiếm sự chăm sóc y tế nếu họ xuất hiện các triệu chứng của sốt xuất huyết hoặc các dấu hiệu cảnh báo sốt xuất huyết.
Không có dữ liệu về việc sử dụng Qdenga® ở các đối tượng trên 60 tuổi và dữ liệu còn hạn chế ở những bệnh nhân bị các tình trạng y khoa mạn tính.
Các phản ứng liên quan đến lo âu
Các phản ứng liên quan đến lo âu, bao gồm phản ứng mạch-thần kinh phế vị (ngất), tăng thông khí hoặc các phản ứng liên quan đến stress có thể xảy ra liên quan đến tiêm chủng như một phản ứng tâm lý đối với kim tiêm. Điều quan trọng là áp dụng các biện pháp phòng ngừa để tránh tổn thương do ngất.
Phụ nữ có khả năng mang thai
Cũng như các vắc-xin sống giảm độc lực khác, phụ nữ có khả năng mang thai nên tránh mang thai trong ít nhất 1 tháng sau khi tiêm chủng.
Khác
Không tiêm tĩnh mạch, tiêm trong da hay tiêm bắp Qdenga®.
10. Dùng cho phụ nữ có thai và cho con bú
Phụ nữ có khả năng mang thai
Phụ nữ có khả năng mang thai nên tránh mang thai trong ít nhất 1 tháng sau khi tiêm chúng.
Nên khuyên phụ nữ có ý định mang thai trì hoãn tiêm chủng.
Phụ nữ có thai
Không có đủ các nghiên cứu về độc tính đối với sinh sản trên động vật.
Dữ liệu còn hạn chế về việc sử dụng Qdenga ở phụ nữ có thai. Các dữ liệu này không đủ để kết luận về việc không có các tác động tiềm ẩn của Qdenga® đối với thai kỳ, sự phát triển của phôi-thai, sự sinh đẻ và phát triển sau sinh.
Qdenga® là vắc-xin sống giảm độc lực, do đó chống chỉ định dùng Qdenga® trong khi mang thai.
Cho con bú
Chưa rõ liệu Qdenga® có được bài tiết vào sữa mẹ hay không. Không thể loại trừ nguy cơ đối với trẻ sơ sinh/trẻ nhỏ.
Chống chỉ định dùng Qdenga trong thời kỳ cho con bú.
11. Ảnh hưởng của thuốc Qdenga lên khả năng lái xe và vận hành máy móc
Qdenga® có ảnh hưởng nhỏ đến khả năng lái xe và vận hành máy móc.
12. Quá liều
Không có trường hợp quá liều nào được báo cáo.
13. Bảo quản
Bảo quản thuốc Qdenga trong tủ lạnh (2 - 8 độ C), không để đông lạnh, bảo quản trong bao bì gốc.
Không để thuốc tiếp xúc với ánh nắng mặt trời.
Không dùng thuốc Qdenga quá hạn ghi trên bao bì.
14. Mua thuốc Qdenga ở đâu?
Hiện nay, Qdenga là thuốc kê đơn, vì vậy bạn cần nói rõ các triệu chứng của bệnh nhân để được nhân viên y tế tư vấn và hỗ trợ. Thuốc có bán tại các bệnh viện hoặc các nhà thuốc lớn.
Mọi người nên tìm hiểu thông tin nhà thuốc thật kỹ để tránh mua phải hàng giả, hàng kém chất lượng, ảnh hưởng đến quá trình điều trị.
Nếu mọi người ở khu vực Hà Nội có thể mua thuốc có sẵn ở nhà thuốc Thanh Xuân 1 - địa chỉ tại Số 1 Nguyễn Chính, phường Tân Mai, quận Hoàng Mai, Hà Nội. Ngoài ra, mọi người cũng có thể gọi điện hoặc nhắn tin qua số hotline của nhà thuốc là: 0325095168 - 0387651168 hoặc nhắn trên website nhà thuốc để được nhân viên tư vấn và chăm sóc tận tình.
15. Giá bán
Giá bán thuốc Qdenga trên thị trường hiện nay dao động trong khoảng tùy từng địa chỉ mua hàng và giá có thể giao động tùy thời điểm. Mọi người có thể tham khảo giá tại các nhà thuốc khác nhau để mua được thuốc đảm bảo chất lượng và giá thành hợp lý nhất.
“Những thông tin trên chỉ mang tính chất tham khảo, mọi người nên đến thăm khám và hỏi ý kiến bác sĩ có kiến thức chuyên môn để sử dụng an toàn và hiệu quả.”