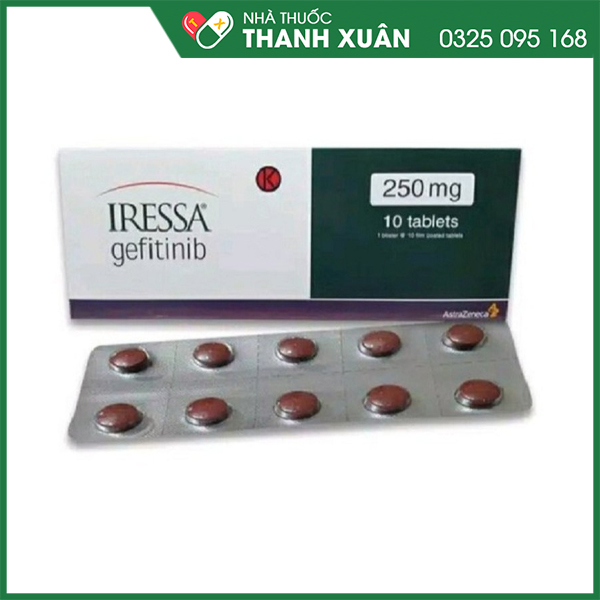
Iressa điều trị cho bệnh nhân người lớn ung thư phổi loại không phải tế bào nhỏ giai đoạn tiến triển tại chỗ hoặc di căn mà có đột biến hoạt hóa EGFR TK.
1. Thuốc Iressa là thuốc gì?
Thuốc Iressa thuốc nhóm thuốc chống ung thư, ức chế protein kinase. Hoạt chất Gefitinib trong thuốc có tác dụng ức chế chọn lọc tyrosine kinase trên thụ thể của yếu tố phát triển biểu bì (epidermal growth factor receptor-EGFR), thường có trong các bướu biểu mô. Khi EGFR tyrosine kinase bị ức chế sẽ làm ức chế sự phát triển, di căn của khối u, hạn chế sự tăng sinh mạch máu mới và thúc đẩy quá trình chết tế bào bướu theo chương trình. Thuốc Iressa được chỉ định cho những bệnh nhân ung thư phổi không tế bào nhỏ
2. Thành phần thuốc Iressa
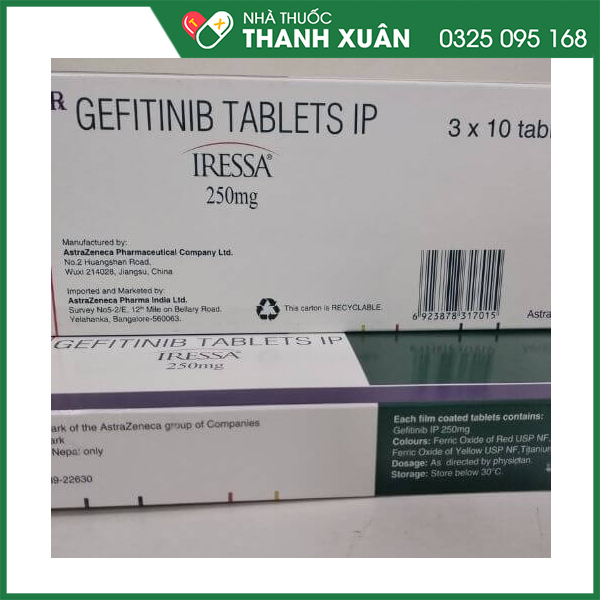
Hoạt chất: Gefitinib ………. 250 mg
Tá dược: Lactose monohydrat, cellulose vi tinh thể, croscarmellose natri, povidon, natri lauryl sulfat, magnesi stearat, hypromellose, macrogol 300, titan dioxyd, oxyd sắt vàng, oxyd sắt đỏ.
3. Dạng bào chế:
Thuốc Iressa được bào chế dưới dạng viên nén bao phim có hai mặt lồi, hình tròn, màu nâu, một mặt có khắc “IRESSA 250” và một mặt trơn.
4. Chỉ định
Thuốc Iressa được chỉ định điều trị cho bệnh nhân người lớn ung thư phổi loại không phải tế bào nhỏ giai đoạn tiến triển tại chỗ hoặc di căn mà có đột biến hoạt hóa EGFR TK.
5. Chống chỉ định
Quá mẫn với hoạt chất hay tá dược.
Phụ nữ đang cho con bú.
6. Tác dụng không mong muốn của thuốc
Tóm tắt dữ liệu an toàn thuốc
Dữ liệu gộp từ các thử nghiệm lâm sàng pha III như ISEL, INTEREST và IPASS (thực hiện trên 2462 bệnh nhân điều trị với IRESSA), các phản ứng ngoại ý do thuốc (ADR) thông thường nhất được ghi nhận xảy ra trên > 20% bệnh nhân là tiêu chảy và phản ứng trên da (bao gồm nổi mẩn, mụn, da khô và ngứa). Các phản ứng ngoại ý do thuốc thường xuất hiện trong tháng đầu điều trị và nói chung có thể tự hết. Khoảng 8% bệnh nhân có phản ứng ngoại ý trầm trọng (độ 3 và 4 theo Tiêu chuẩn Đánh giá Độc tính Thường gặp - CTC: Common Toxicity Criteria). Tuy nhiên, chỉ có 3% bệnh nhân là phải ngưng điều trị do phản ứng ngoại ý.
Bệnh phổi mô kẽ (ILD) xảy ra ở 1,3% bệnh nhân, thường gặp mức độ nghiêm trọng (độ 3-4 theo theo Tiêu chuẩn Đánh giá Độc tính Thường gặp). Cũng có ghi nhận hậu quả là tử vong.
Bảng phân loại phản ứng ngoại ý
Dữ liệu an toàn thuốc trình bày trong Bảng 7 được dựa trên các chương trình phát triển lâm sàng của gefitinib. Phản ứng ngoại ý được sắp xếp theo cột tần số ở Bảng 7 nếu có thể dựa trên tỷ lệ các báo cáo phản ứng ngoại ý có thể so sánh được trong dữ liệu gộp từ các thử nghiệm lâm sàng pha III như ISEL, INTEREST và IPASS (trên 2462 bệnh nhân điều trị với IRESSA).
Tần số xảy ra các phản ứng ngoại ý được xác định như sau: rất thường gặp (≥1/10); thường gặp (≥1/100 - <1/10); ít gặp (≥1/1.000 - <1/100); hiếm gặp (≥1/10.000 - <1/1.000); rất hiếm gặp (<1/10.000), chưa biết (không thể dự đoán từ các dữ liệu sẵn có).
Trong mỗi nhóm phân loại, các phản ứng ngoại ý được sắp xếp theo trình tự mức độ giảm dần.
- xem Bảng 7.
Bệnh phổi mô kẽ (ILD)
Trong nghiên cứu lâm sàng INTEREST, tỷ lệ các loại phản ứng ngoại ý là 1,4% (10) bệnh nhân trong nhóm gefitinib so với 1,1% (8) bệnh nhân trong nhóm docetaxel. Một phản ứng ngoại ý loại bệnh phổi mô kẽ gây tử vong và đã xảy ra ở một bệnh nhân thuộc nhóm gefitinib.
Trong nghiên cứu lâm sàng ISEL, tần suất biến cố loại ILD ở toàn bộ bệnh nhân là tương tự nhau và khoảng 1% ở cả 2 nhánh điều trị. Đa số biến cố loại ILD ghi nhận là ở bệnh nhân thuộc chủng tộc Châu Á và tần suất xảy ra ILD giữa nhóm bệnh nhân Châu Á điều trị bằng IRESSA và nhóm dùng giả dược là khoảng 3% và 4 % theo thứ tự tương ứng. Có 1 bệnh nhân thuộc nhóm dùng giả dược có biến cố ILD tử vong.
Trong một nghiên cứu theo dõi sau khi đưa thuốc ra thị trường tại Nhật (3350 bệnh nhân), tỷ lệ biến cố loại ILD được ghi nhận ở bệnh nhân dùng gefitinib là 5,8%. Tỷ lệ của các phản ứng ngoại ý loại ILD bị tử vong là 38,6%.
Trong thử nghiệm lâm sàng nhãn mở pha III (IPASS) trên 1217 bệnh nhân so sánh IRESSA với hóa trị liệu 2 thuốc carboplatin/paclitaxel như là điều trị bước đầu ở những bệnh nhân ung thư phổi không phải tế bào nhỏ giai đoạn tiến triển tại châu Á, tỷ lệ biến cố loại ILD là 2,6% ở nhóm điều trị với IRESSA so với 1,4% ở nhóm điều trị với carboplatin/paclitaxel.
7. Tương tác thuốc
Gefitinib chuyển hóa qua cytochrom P450, chủ yếu là isoenzym CYP3A4 và qua CYP2D6.
Các thuốc có thể làm tăng nồng độ gefitinib trong máu
Các nghiên cứu in-vitro cho thấy gefitinib là một chất nền của glycoprotein. Các dữ liệu hiện nay không có chỉ ra bất kỳ mối liên quan lâm sàng với phát hiện in-vitro này.
Các thuốc ức chế CYP3A4 có thể làm giảm độ thanh thải của gefitinib. Sử dụng đồng thời với các thuốc ức chế mạnh hoạt động của CYP3A4 (như ketoconazol, posaconazol, voriconazol, thuốc ức chế enzym protease, clarithromycin, telithromycin) có thể làm tăng nồng độ gefitinib trong huyết tương. Sự gia tăng này có thể có ý nghĩa về mặt lâm sàng vì đã ghi nhận các phản ứng ngoại ý liên quan đến liều và nồng độ thuốc trong cơ thể.
Sự gia tăng này có thể cao hơn ở cá thể bệnh nhân có kiểu gen chuyển hóa qua CYP2D6 giảm. Điều trị trước với itraconazol (một thuốc ức chế CYP3A4 mạnh) đã làm tăng 80% trị số AUC trung bình của gefitinib ở người tình nguyện khoẻ mạnh. Nếu dùng đồng thời với thuốc ức chế CYP3A4, nên theo dõi chặt chẽ các phản ứng ngoại ý của gefitinib.
Chưa có dữ liệu về việc điều trị đồng thời với thuốc ức chế CYP2D6 nhưng các thuốc ức chế mạnh enzym này có thể làm tăng nồng độ gefitinib trong huyết tương khoảng 2 lần ở các bệnh nhân có chuyển hóa mạnh qua CYP2D6. Nếu dùng đồng thời với thuốc ức chế mạnh CYP2D6, nên theo dõi chặt chẽ các phản ứng ngoại ý trên bệnh nhân.
Các thuốc làm giảm nồng độ gefitinib trong huyết tương
Các thuốc cảm ứng CYP3A4 có thể làm tăng chuyển hóa và làm giảm nồng độ gefitinib trong huyết tương và vì thế làm giảm hiệu lực của gefitinib. Nên tránh sử dụng đồng thời với các thuốc cảm ứng CYP3A4 (như phenytoin, carbamazepin, rifampicin, barbiturat hoặc cỏ St John's wort (Hypericum perforatum)). Điều trị trước với rifampicin (thuốc cảm ứng CYP3A4 mạnh) ở người tình nguyện khỏe mạnh làm giảm khoảng 83% trị số AUC trung bình (xem phần Cảnh báo và thận trọng).
Các thuốc làm tăng đáng kể nồng độ pH dịch vị có thể làm giảm nồng độ gefitinib trong huyết tương và vì thế làm giảm hiệu lực của gefitinib. Liều cao các thuốc kháng acid tác động ngắn có thể có tác động tương tự nếu dùng thường xuyên sát thời điểm dùng gefitinib. Dùng đồng thời gefitinib với ranitidin ở mức liều làm tăng kéo dài pH dịch vị ≥5 dẫn đến giảm khoảng 47% trị số AUC trung bình ở người tình nguyện khỏe mạnh (xem phần Cảnh báo và thận trọng và Đặc tính dược lực học).
Các thuốc bị thay đổi nồng độ trong huyết tương do ảnh hưởng của gefitinib
Các nghiên cứu in-vitro cho thấy gefitinib ít có khả năng ức chế CYP2D6. Trong một thử nghiệm lâm sàng, gefitinib được dùng đồng thời với metoprolol (một chất nền của CYP2D6). Điều này làm tăng 35% nồng độ và thời gian tiếp xúc với metoprolol. Việc gia tăng này có ý nghĩa với các chất nền CYP2D6 có chỉ số điều trị hẹp. Cân nhắc khi sử dụng các chất nền CYP2D6 phối hợp với gefitinib, cần điều chỉnh liều của chất nền CYP2D6, đặc biệt là các thuốc có cửa sổ trị liệu hẹp.
Gefitinib ức chế protein vận chuyển BCRP in-vitro, nhưng vẫn chưa rõ các mối liên quan trên lâm sàng với phát hiện này.
Các khả năng tương tác khác: Tăng INR và/hoặc các biến cố xuất huyết đã được báo cáo ở một vài bệnh nhân dùng warfarin (xem phần Cảnh báo và thận trọng).
8. Cảnh báo và thận trọng khi dùng thuốc Iressa
Khi xem xét sử dụng IRESSA để điều trị cho bệnh nhân ung thư phổi loại không phải tế bào nhỏ giai đoạn tiến triển hoặc di căn, khuyến cáo xét nghiệm đánh giá đột biến EGFR tại mô khối u cho tất cả các bệnh nhân. Nếu mẫu khối u không thể đánh giá được, thì có thể sử dụng mẫu DNA của khối u trong hệ tuần hoàn (ctDNA) thu thập từ mẫu máu (huyết tương). Chỉ dùng các phương pháp xét nghiệm có độ tái lặp, độ tin cậy, độ nhạy cùng với tiện ích đã được chứng minh về xác định tình trạng đột biến EGFR của khối u hay ctDNA để tránh kết quả âm tính giả hay dương tính giả (xem phần Đặc tính dược lực học).
Bệnh phổi mô kẽ (ILD)
Bệnh phổi mô kẽ, có thể khởi phát cấp tính, đã được quan sát thấy ở 1,3% bệnh nhân đang dùng gefitinib, và một vài trường hợp có thể bị tử vong (xem phần Tác dụng không mong muốn). Nếu bệnh nhân có biểu hiện xấu đi với các triệu chứng hô hấp như khó thở, ho và sốt, nên ngừng IRESSA và cho kiểm tra ngay. Nếu xác nhận chẩn đoán là bệnh phổi mô kẽ, nên ngưng dùng IRESSA và điều trị bệnh nhân bằng các biện pháp thích hợp.
Trong một nghiên cứu dược lý dịch tễ có đối chứng tại Nhật thực hiện trên 3159 bệnh nhân ung thư phổi loại không tế bào nhỏ (NSCLC) đã được theo dõi trong 12 tuần khi dùng gefitinib hoặc hóa trị, các yếu tố nguy cơ phát triển bệnh phổi mô kẽ (ILD) như sau đã được xác định (bất kể bệnh nhân dùng IRESSA hoặc hóa trị) là: hút thuốc, tình trạng thể chất kém (PS ≥2), giảm thể tích phổi bình thường có chứng cứ chụp cắt lớp CT (≤ 50%), mới được chẩn đoán NSCLC (<6 tháng), bệnh phổi mô kẽ (ILD) có sẵn trước, lớn tuổi (≥55 tuổi) và bệnh tim đồng thời. Đã ghi nhận gia tăng nguy cơ bệnh phổi mô kẽ ở nhóm dùng gefitinib so với hóa trị chủ yếu trong vòng 4 tuần đầu sử dụng (giá trị OR hiệu chỉnh 3,8; 95% Cl 1,9-7,7); sau đó nguy cơ tương đối thấp hơn (giá trị OR hiệu chỉnh 2,5; 95% Cl 1,1-5,8). Trong số bệnh nhân bị ILD ở cả 2 nhóm IRESSA và hóa trị thì nguy cơ tử vong cao ở nhóm bệnh nhân có các yếu tố nguy cơ sau: hút thuốc, giảm thể tích phổi bình thường có chứng cứ chụp cắt lớp CT (≤ 50%), bệnh phổi mô kẽ (ILD) có sẵn trước, lớn tuổi (≥65 tuổi) và các vùng dính liền với màng phổi quá rộng (≥ 50%).
Ngộ độc gan và suy giảm chức năng gan
Bất thường xét nghiệm chức năng gan (bao gồm tăng alanin aminotransferase, aspartat aminotransferase, bilirubin) đã được ghi nhận nhưng ít khi có biểu hiện viêm gan (xem phần Tác dụng không mong muốn). Vài báo cáo riêng lẻ suy chức năng gan mà một số trường hợp dẫn đến tử vong. Vì vậy, bệnh nhân được khuyến cáo nên kiểm tra chức năng gan định kỳ. Gefitinib nên được dùng thận trọng trên bệnh nhân có thay đổi chức năng gan ở mức độ nhẹ hoặc trung bình. Cân nhắc ngưng sử dụng thuốc nếu các thay đổi là nghiêm trọng.
Suy giảm chức năng gan do xơ gan đã được ghi nhận là dẫn đến tăng nồng độ gefitinib trong huyết tương (xem phần Đặc tính dược lực học).
Tương tác với các thuốc khác
Các chất gây cảm ứng với hệ enzym CYP3A4 có thể làm tăng chuyển hóa gefitinib và giảm nồng độ gefitinib trong huyết tương. Vì vậy, khi phối hợp với các chất gây cảm ứng CYP3A4 (như phenytoin, carbamazepin, rifampicin, barbiturat hoặc chế phẩm từ dược liệu có chứa St John’s Wort/Hypericum perforatum) có thể làm giảm hiệu lực của thuốc và vì thế nên tránh sử dụng chung các thuốc này (xem phần Tương tác).
Ở các bệnh nhân có kiểu gen chuyển hóa qua CYP2D6 giảm, điều trị bằng thuốc ức chế mạnh CYP3A4 có thể dẫn đến tăng nồng độ của gefitinib trong huyết tương. Khi bắt đầu điều trị bằng thuốc ức chế CYP3A4, bệnh nhân cần được theo dõi chặt chẽ các phản ứng ngoại ý của gefitinib (xem phần Tương tác).
Tăng INR (International Normalised Ratio) và/hoặc các biến cố xuất huyết đã được báo cáo ở một số bệnh nhân đang dùng warfarin (xem phần Tương tác). Nên thường xuyên theo dõi sự thay đổi về thời gian prothrombin (PT) hoặc INR ở bệnh nhân đang dùng warfarin.
Các thuốc làm tăng đáng kể và kéo dài độ pH dịch vị như thuốc ức chế bơm proton và thuốc đối kháng thụ thể H2 có thể làm giảm sinh khả dụng và nồng độ gefitinib trong huyết tương và vì thế có thể giảm hiệu lực của thuốc. Thuốc kháng acid nếu dùng thường xuyên gần thời điểm uống thuốc gefitinib có thể có tác động tương tự (xem phần Tương tác và Đặc tính Dược động học).
Dữ liệu từ các nghiên cứu lâm sàng pha II, khi dùng đồng thời gefitinib và vinorelbin cho thấy gefitinib có thể làm tăng tác động giảm bạch cầu trung tính của vinorelbin.
Lactose
IRESSA có chứa lactose. Bệnh nhân có vấn đề di truyền hiếm gặp kém dung nạp galactose, thiếu hụt lactose tổng hoặc kém hấp thu glucose-galactose thì không nên dùng thuốc này.
Các thận trọng khác
Nên khuyên bệnh nhân khám bác sỹ ngay lập tức khi có tiêu chảy trầm trọng hoặc dai dẳng, buồn nôn, nôn hoặc biếng ăn mà có thể gián tiếp dẫn tới mất nước cơ thể. Các triệu chứng này có thể được xử trí theo bệnh cảnh lâm sàng (xem phần Tác dụng không mong muốn).
Bệnh nhân có các dấu hiệu và triệu chứng nghi ngờ viêm giác mạc như tình trạng cấp tính hay trầm trọng hơn: viêm mắt, tuyến lệ, mẫn cảm với ánh sáng, nhìn mờ, đau mắt và/hoặc đỏ mắt nên nhanh chóng tham vấn bác sĩ chuyên khoa mắt.
Nếu chẩn đoán đã xác định là viêm loét giác mạc, nên ngưng điều trị với gefitinib và nếu các triệu chứng không hết hẳn hoặc tái phát khi sử dụng lại gefitinib, cân nhắc ngưng sử dụng lâu dài gefitinib.
Trong một nghiên cứu pha I/II sử dụng gefitinib và xạ trị ở bệnh nhân nhi mới được chẩn đoán u thần kinh đệm cuống não (brain stem glioma) hoặc u thần kinh đệm ác tính trên lều đã được cắt bỏ không hoàn toàn (incompletely resected supratentorial malignant glioma), có 4 trường hợp xuất huyết ở hệ thần kinh trung ương (trong đó có 1 trường hợp tử vong) đã được ghi nhận trong 45 bệnh nhân tham gia nghiên cứu. Một trường hợp xuất huyết ở hệ thần kinh trung ương ở trẻ u màng não thất (ependymoma) cũng được ghi nhận trong thử nghiệm dùng gefitinib đơn thuần. Việc tăng nguy cơ xuất huyết não ở bệnh nhân trưởng thành bị ung thư phổi loại không phải tế bào nhỏ dùng IRESSA chưa được thiết lập.
Đã có ghi nhận thủng dạ dày ruột ở bệnh nhân dùng gefitinib. Trong đa số các trường hợp, điều này có liên quan đến các yếu tố nguy cơ đã biết khác, bao gồm tuổi cao, sử dụng đồng thời các thuốc khác như steroid, kháng viêm NSAID, bệnh nền loét dạ dày ruột, hút thuốc hoặc di căn ở ruột tại vị trí thủng.
9. Sử dụng thuốc cho phụ nữ mang thai và cho con bú
Phụ nữ mang thai:
Chưa có dữ liệu về việc dùng gefitinib cho phụ nữ có thai. Các nghiên cứu trên động vật đã chứng tỏ thuốc có độc tính trên hệ sinh sản. Chưa biết khả năng nguy cơ đối với con người. Không nên dùng IRESSA trong thai kỳ trừ khi thật sự rất cần thiết.
Phụ nữ cho con bú:
Hiện vẫn chưa biết liệu gefitinib có bài tiết qua sữa ở người hay không. Gefitinib và các chất chuyển hóa của gefitinib đi vào sữa của chuột thí nghiệm. Chống chỉ định dùng gefitinib trong khi đang cho con bú và vì thế phụ nữ đang cho con bú phải ngưng cho con bú trong khi điều trị bằng IRESSA (xem phần Chống chỉ định).
Khả năng sinh sản
Khuyến cáo phụ nữ trong độ tuổi sinh sản không nên có thai trong quá trình điều trị với thuốc này.
10. Ảnh hưởng lên khả năng lái xe và vận hành máy móc
Đã có báo cáo về triệu chứng suy nhược trong khi điều trị bằng gefitinib. Do đó, các bệnh nhân có triệu chứng này nên thận trọng khi lái xe hoặc vận hành máy.
11. Bảo quản
Cần phải bảo quản thuốc Iressa ở nơi khô ráo, nhiệt độ không quá 30 độ C tránh ánh sáng trực tiếp.
Không dùng quá hạn ghi trên bao bì
Để xa tầm tay trẻ em.
12. Mua thuốc Iressa ở đâu?
Thuốc Iressa có bán tại các bệnh viện hoặc các nhà thuốc trên toàn quốc. Tuy nhiên khách hàng nên lựa chọn cho mình những địa điểm mua chính hãng để đạt được hiệu quả tốt nhất trọng nhất trong quá trình điều trị. Nếu mọi người ở khu vực Hà Nội có thể mua thuốc có sẵn ở nhà thuốc Thanh Xuân 1 - địa chỉ tại Số 1 Nguyễn Chính, phường Tân Mai, quận Hoàng Mai, Hà Nội. Ngoài ra, mọi người cũng có thể gọi điện hoặc nhắn tin qua số hotline của nhà thuốc là: 0325095168 hoặc nhắn trên website nhà thuốc để được nhân viên tư vấn và chăm sóc tận tình.
13. Giá bán
Giá bán thuốc Iressa trên thị trường hiện nay dao động trong khoảng . Tuy nhiên giá thuốc có thể thay đổi phụ thuộc vào địa điểm mua hàng cũng như tùy từng thời điểm.
“Những thông tin trên chỉ mang tính chất tham khảo, mọi người nên đến thăm khám và hỏi ý kiến bác sĩ, dược sĩ có kiến thức chuyên môn để sử dụng an toàn và hiệu quả.”